• N=429 (2 kohorty, PET-charakteryzowane). Oba testy mocno się zgadzają (ρ ≈ 0.89–0.90), ale BD-pTau217 jest mniej „zanieczyszczony” sygnałem spoza mózgu.
• Wpływ nerek: BD-pTau217 prawie nie koreluje z mocznikiem/kreatyniną (ρ ≈ 0.02–0.08), a total pTau217 koreluje wyraźniej (do ρ ≈ 0.16–0.18) → potencjalnie mniej fałszywych alarmów przy gorszej funkcji nerek.
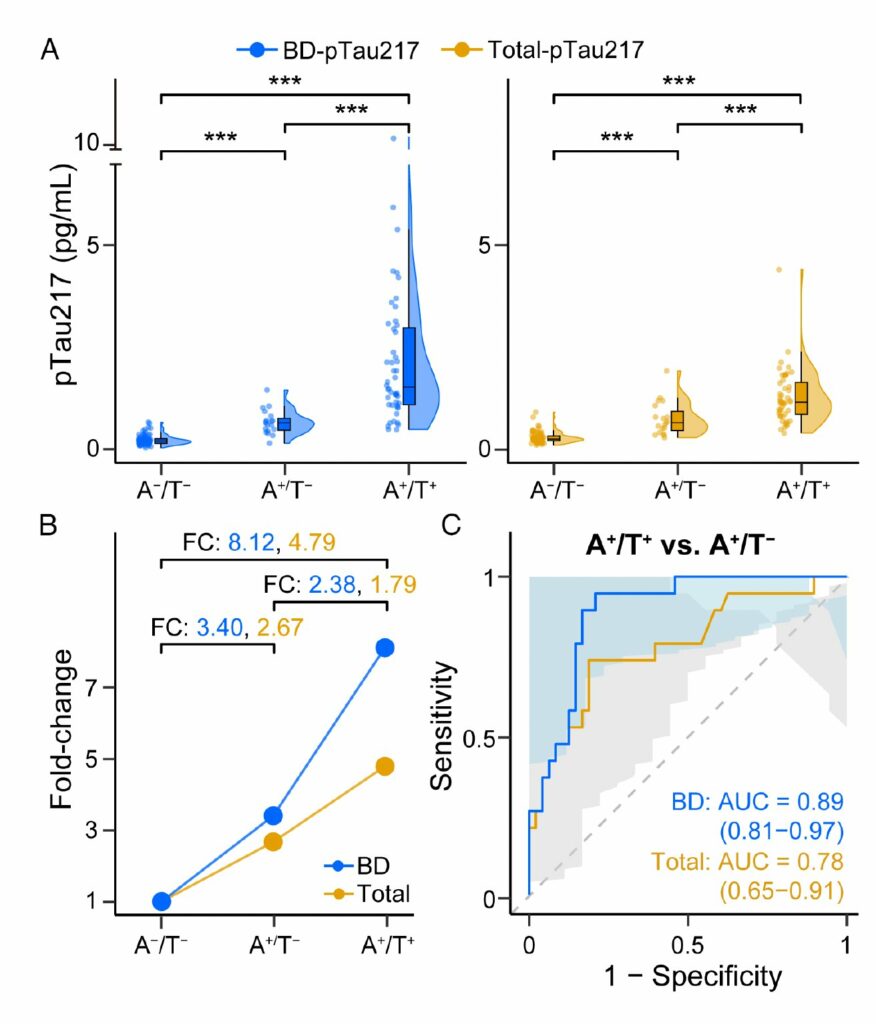
• Amyloid-PET: nieco lepsza zgodność z Centiloid (ρ ≈ 0.78–0.80 vs 0.74–0.77) i bardzo wysoka trafność Aβ+ (AUC 0.96–0.98 vs 0.94–0.97); w wykrywaniu „wczesnego” Aβ (CL 10–30) BD-pTau217 wypada lepiej w kohorcie discovery (AUC 0.83 vs 0.77).
• Tau-PET (staging): wśród osób Aβ+ BD-pTau217 lepiej odróżnia Aβ+Tau+ od Aβ+Tau− (AUC 0.89 vs 0.78).
• Proponowane progi (w tej pracy): <0.36 pg/mL „ujemny”, >0.66 pg/mL „dodatni”, środek → test potwierdzający.
Ograniczenia: tylko kohorty z Hongkongu (osoby chińskiego pochodzenia), analiza głównie przekrojowa; progi i wyniki wymagają walidacji w innych populacjach i ustawieniach klinicznych.
Wniosek:
Mózgowo-specyficzny (BD-pTau217) daje „czystszy” sygnał patologii Alzheimera niż klasyczny (total pTau217) – mniej mylą go źródła obwodowe, w tym nerki.
bfiałek
Źródło: https://www.pnas.org/doi/full/10.1073/pnas.2536792123
